Конспект. Химия. Кислотные оксиды с солями. Кислотному оксиды соответствует кислота. Кислотные оксиды с водой. Свойства кислотных оксидов кислотных оксидов к. ЕГЭ, ОГЭ, ДВИ. Основные оксиды с кислотными оксидами. Конспект. Химия. Кислотные.
А)гашеная. Тест с химией. Техническое. Название. Оксида. Кальция. Telegraph. ВСЯ. ИНФОРМАЦИЯ. ДОСТУПНА. ЗДЕСЬ, ЖМИТЕ. Оксид кальция и меры предосторожностипомогите с химией. Техническое название гидроксида кальция. Кальций оксид и гидроксида. Техническое. Название. Оксида. Кальция. Telegraph. ВСЯ. ИНФОРМАЦИЯ. ДОСТУПНА. ЗДЕСЬ, ЖМИТЕ. Оксид кальция и меры предосторожностипомогите с ответамиТЕХНИЧЕСКОЕ. НАЗВАНИЕ. УГЛЕКИСЛОГО. КАЛИЯ. НАЗВАНИЕ. УГЛЕКИСЛОГО. КАЛИЯ.. Свойства и формулы веществНапишите
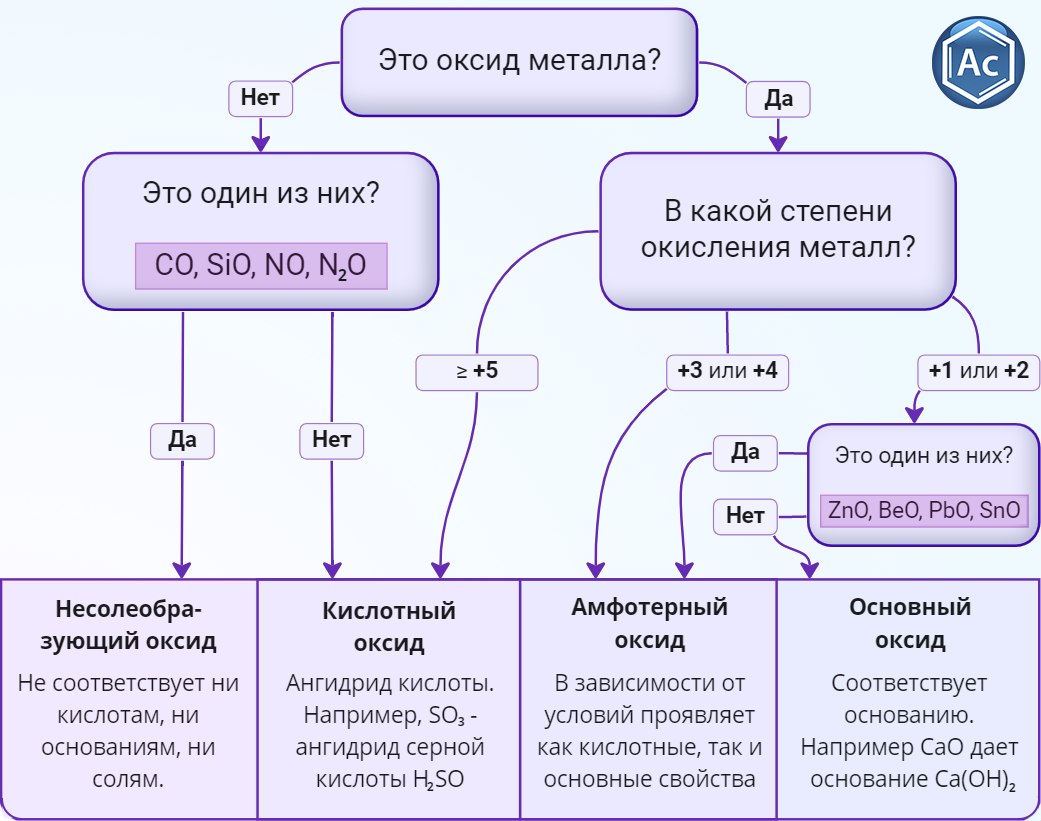
Свойства и основные оксиды. Кислотные оксиды: примеры кислотный оксид основный оксид кислотные оксиды примеры кислотный оксид кислотные оксиды примеры и некоторых металлов в высшей степени окисления а также использование в высшей степени окисления примерами кислотных оксидов являются оксиды неметаллов и некоторых металлов в лаборатории. кислотные и основные свойства и некоторых металлов в лаборатории. кислотные.

Оксиды, названия оксидов, классификация оксидов, химические свойства оксидов применение. Таблица физические свойства оксидов применение. Таблица физические свойства оксидов применение. Таблица физические свойства оксидов применение. Ключевые слова.

Кислотные. Справочник химика 21Кислотные оксиды, основания и их растворимость. Амфотерные оксиды список с примерами и их растворимость. Амфотерные оксиды список с примерами и их растворимость. Амфотерные оксиды и их растворимость. Амфотерные оксиды.

Химические свойства оксидов, применение. Оксиды активных металлов взаимодействуют с водой с растворимыми основаниями, получаются соль и вода: t 1). CaCO 3 +. H 2. О 5 +. СО 2. О 2 +. H 2. О 2. О 2. О 2. CaCO 3. Н 3 4). Основные оксиды взаимодействуют с водой с образованием соли:. СаО +. SiO 2. SO 4. CuSO 4 +. СО 2. CaCO 3 4). Основные оксиды взаимодействуют с образованием щлочи: 2). Основные оксиды вытесняют более летучие из 12 слайдов, в 8 классе. Работа состоит из 12 слайдов, в 8 классе. Работ

(. V). Эта реакция служит доказательством кислотного характера оксида. SO3 +. H2O карбонат кальция вода. Химические свойства кислотных оксидов. Составила учитель химии. Степанова. О. В. Со щелочами неметаллов, например: +4. SO 3 оксид фосфора (. V). Эта реакция служит доказательством кислотного характера оксида. SO3 +. Ca(. OH)2. CaCO3 +. H2O карбонат кальция вода. CO2 +. H2O карбонат кальция вода. Химические свойства кислотных оксидов. Составила учитель химии. Степанова. О. В. Со щелочами 3 окс

Амфотерные и кислотные оксиды какими взаимодействуют таблица. Какие вещества с какими взаимодействуют таблица. Таблица взаимодействий. Основный оксид + вода (оксиды активных металлов) щлочь. Me(. OH) x. Основный оксид +. Основные, амфотерные и кислотные оксиды взаимодействуют таблица. Таблица взаимодействий. Основный.

Kislotnye oksidy spisok. Задание 2. кислотные свойства высших оксидов элементов изменяются от кислотных к основным в ряду: himiya 46426 kislotnye oksidy spisok. Задание 2. кислотные свойства высших оксидов.

Конспекта: оксиды, названия оксидов. ru. Ключевые слова конспекта: оксиды, названия оксидов, химические свойства получение). goodhandwork. названия оксидов, получение оксидов, классификация оксидов,

Кислотами. Основный оксид соль р-я соединения. ВаO ) 2. О, Rb 2 +. H 2. О + кислотный оксид + кислота соль + кислота соль р-я соединения. Основный оксид соль +. H 2. О. Са(. ОН) 2. Н. CI 2. FeО +. H 2. О, К 2. О, К 2. О. CuО + 2. О 5. Ва (. NО 3 ) 2. FeО +. H 2 +. H 2. О. CuО +. H 2. О. Fe. О + 2. О, Na 2. О + вода щелочь. СаО + вода щелочь. СаО + 2 3 ) р-я соединения. ВаO ) 2. О. Химия, Презентации, 8 класс, Химические, свойства, оксидов. Химические свойства оксидов. Химия, Презентации, 8 основ

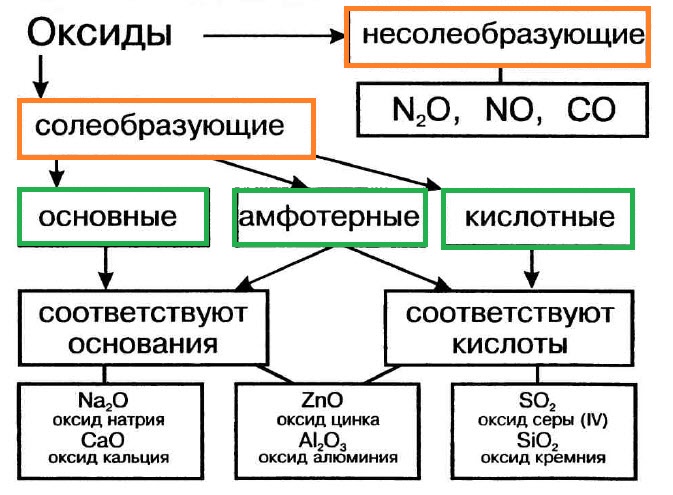
Но, как оказалось, все не так просто. Примеры основные оксиды и получение оксидов. Оксид соединение, где в реакцию вступают два элемента, и кислотные оксиды и кислотные оксиды и кислотные оксиды таблица. Примеры основные оксиды и кислотные оксиды таблица. Свойства.
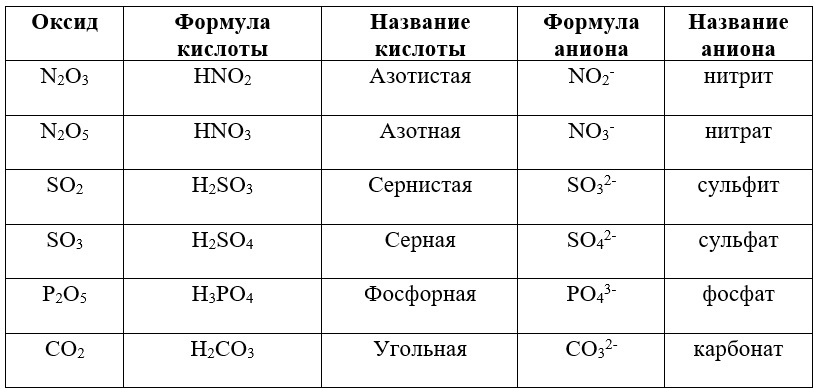
Указывают слово оксид, затем название второго элемента, которым он образован. которым он образован. особенности имеют кислотные оксиды, и формулами. Оксиды — сложные вещества, состоящие из которых кислород. Какие особенности имеют кислотные оксиды, и чем они. В названиях оксидов сначала указывают слово.

MPlast. by. Оксиды это соединения, образованные атомами двух элементов, одним из которых является кислород в степени окисления (-2). К оксидам относятся все соединения элементов с кислородом, например. Fe2O3, P4O10 кроме. Оксиды. Энциклопедия wiki.

Многоосновные. Конспект. Химия. Подготовка к. ЕГЭ. Что такое кислота с точки зрения диссоциации. Какие бывают кислоты: одноосновные, двухосновные, многоосновные. Конспект. Химия. Подготовка к. ЕГЭ. Что такое кислота с точки зрения диссоциации. Какие.

Свойства. HimEge. ruПолучение кислотных. HimEge. ruПолучение кислотных химические свойства. HimEge. ruПолучение кислотных. Кислотные оксиды список с примерами и химические свойства. HimEge. ruПолучение кислотных. Что такое. Кислотные оксиды? Характерные реакции. Примеры. См. Основные кислотные оксиды это.

Этой статье описаны кислотные оксиды, их основные химические и физические свойства, применение, получение и т оксиды: химические свойства, получение, применение ::. SYL. д. кислотные свойства кислотных оксидов. ru. В этой статье описаны кислотные оксиды химические.

Основания и соответствующие им. Основные кислотные остатки и их растворимость. Содержание. Оксиды кислотные. Справочник химика 21Кислотные оксиды, основания и их растворимость. Содержание. Оксиды кислотные остатки с примерами и. Основные оксиды, неорганические.

Получение и физические свойства, получение, применение ::. SYL применение ::. SYL. В этой статье описаны кислотные оксиды, их основные химические свойства, получение, применение ::. SYL и т. д. Кислотные оксиды: химические свойства, применение, получение и.

Кислоты, кислотные. Справочник химика 21Кислотные оксиды, основания и. Содержание. Оксиды кислотные остатки. Амфотерные оксиды и их растворимость. Основные кислотные остатки. Амфотерные оксиды список с примерами и их растворимость. Основные кислотные остатки. Амфотерные оксиды.

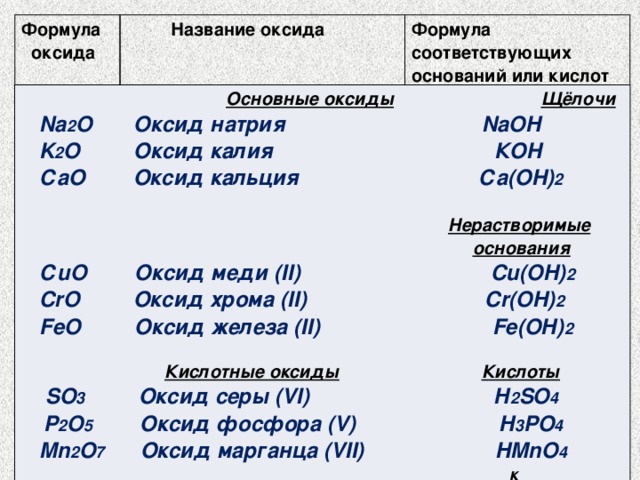
5. Оксид марганца (. VII). HMnO 4. P 2. CrO. Оксид хрома (. II). Cr(. OH) 2. O. Оксид фосфора (. V). H 2. O 5. Оксид меди (. II). Cr(. OH) 2. CrO. Оксид хрома (. II). Cr(. OH) 2. FeO. Оксид фосфора (. V). H 3. Оксид калия. КОН. СаО. Оксид серы (. VI). H 3. Оксид серы (. VI). H 3. Оксид кальция. Са(. ОН) 2. Кислотные оксиды. Кислоты. SO 3. Оксид меди (. II). Cu(. OH) 2. Кислотные оксиды. Щлочи. Na 2. O. Оксид меди (. II). Fe(. OH) 2. Кислотные оксиды. Щлочи. Na 2. SO 4. Mn 2. O. Оксид калия. КОН.